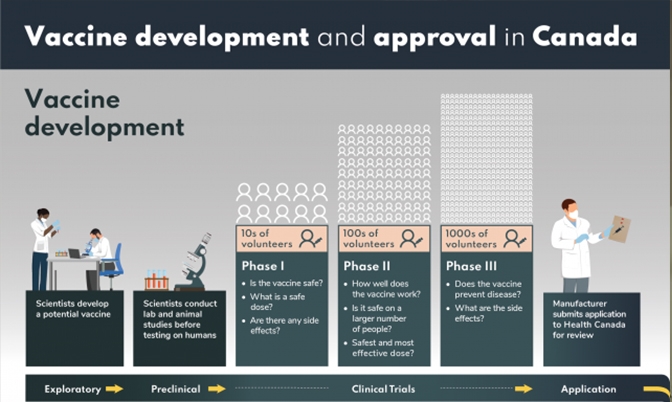
加拿大卫生部关于第一款COVID-19 疫苗的声明:得益于科学技术的进步以及前所未有的全球合作,加拿大今天批准了第一款 COVID-19 疫苗,从而实现了抗击 COVID-19 疫情的一个关键性里程碑。加拿大卫生部于 2020 年 10 月 9 日收到了辉瑞(Pfizer)公司的提交申请,经过对相关证据 进行彻底、独立的审核之后,加拿大卫生部确定辉瑞-BioNTech 的疫苗符合卫生部严格的 安全、功效和质量要求,可以在加拿大使用。
作为政府对开放性和透明度的持续承诺的一部分,加拿大卫生部将公布与该决定相关的多 项文件,其中包括加拿大卫生部审核相关证据的重点摘要,该审核支持对这种疫苗的批准。 未来几周还将提供更多详细信息,包括详细的科学摘要和完整的临床试验数据包。加拿大人可以具有信心,这一审核过程是严格的,并且我们拥有强有力的监控体制。一旦 疫苗投放市场,加拿大卫生部和加拿大公共卫生署将密切监察这种疫苗的安全性,如果发 现任何安全隐患,将毫不犹豫地采取行动。
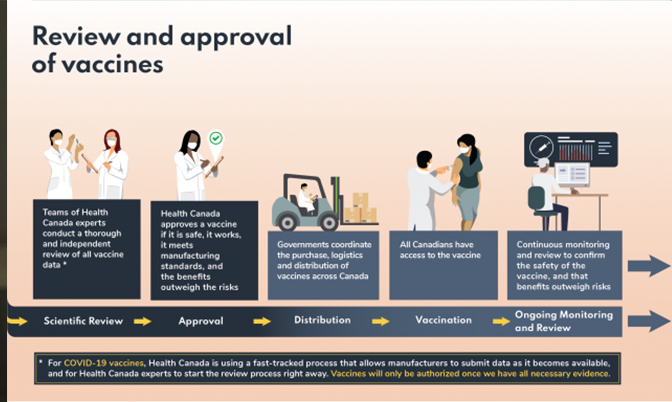
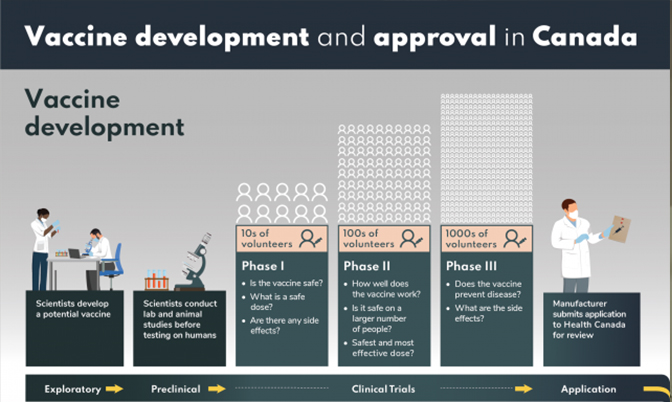
批准辉瑞-BioNTech 疫苗的条款和条件要求制造商继续向加拿大卫生部提供有关疫苗的安 全性、功效和质量的信息,以确保市场使用继续证明这种疫苗的益处。
该疫苗最初的适应症是适用于 16 岁以上的人群。辉瑞-BioNTech 正在针对所有年龄段的 儿童进行进一步的临床测试,如果这些研究的数据支持,这个适应症的范围将来可能会进 行修订以包括儿童。此款疫苗依照加拿大卫生部《关于进口、销售和广告与 COVID-19 相关药物的临时指令》而 予以批准。这个审核过程使得加拿大卫生部可以在产品开发过程中对制造商所提供的信息 进行评估,同时坚持加拿大的高标准。